
|
ENCYCLOPÉDIE DE LA RADIOÉLECTRONIQUE ET DU GÉNIE ÉLECTRIQUE Caractéristiques comparatives des éléments galvaniques de taille AA. Encyclopédie de l'électronique radio et de l'électrotechnique
Encyclopédie de l'électronique radio et de l'électrotechnique / Chargeurs, batteries, cellules galvaniques Aujourd'hui, dans les magasins et les marchés, vous pouvez trouver de nombreuses cellules galvaniques différentes. Lesquels choisir ? Cet article vous aidera à prendre la bonne décision. Les cellules et batteries galvaniques sont largement utilisées pour alimenter divers équipements électroniques. Les éléments de taille AA sont les plus largement utilisés. Sur les étagères, vous pouvez trouver des produits similaires de différentes entreprises, principalement deux systèmes électrochimiques : salin et alcalin. Plus récemment, Energizer a lancé des piles au lithium 1,5 V AA. La caractéristique la plus importante d'une cellule galvanique - la capacité (la quantité d'électricité qu'elle est capable de fournir à la charge) - n'est presque jamais indiquée sur l'étiquette. L'acheteur doit se concentrer sur les publicités télévisées sur les piles qui "fonctionnent jusqu'à dix fois plus longtemps que le sel conventionnel", ou prendre la parole d'Energizer, qui prétend que ses nouvelles piles AA au lithium e2 durent cinq fois plus longtemps que les alcalines conventionnelles [1 ]. De plus, il n'est pas tout à fait clair quels éléments sont appelés "ordinaires". Afin de comparer quantitativement les paramètres d'éléments de différents systèmes électrochimiques, il est nécessaire de les tester dans les mêmes conditions. De tels tests ont été effectués avec trois types de cellules: sel Philips Long Life (emf d'une cellule "fraîche" - 1,65 V), alcaline Duracell Ultra M1,62 (2 V) et lithium Energizer e1,8 (15 V). Chacun d'eux était chargé d'une résistance de 100 ohms, ce qui correspond à un courant de décharge initial d'environ 1 mA. Pour les éléments de taille AA, un tel courant de charge est typique. La décharge a été effectuée par cycles de plusieurs heures par jour, ce qui correspond aux conditions réelles d'exploitation. Ceci explique les pics de tension dans les courbes de décharge illustrées aux Fig. XNUMX. La courbe bleue correspond à l'élément sel, rouge - alcalin et vert - lithium. Pendant le "repos", la tension sur l'élément de tout type a légèrement augmenté, mais après la connexion de la charge, elle a rapidement diminué jusqu'au minimum du cycle précédent. Les points marquent les valeurs de l'EMF des éléments - les tensions sur eux sans charge.
Si nous prenons comme critère de décharge complète de la cellule une diminution de la tension à sa charge à 0,9 V, la capacité déterminée expérimentalement de la cellule au sel était de 1 Ah, la cellule alcaline - 2,9 Ah et la cellule au lithium - 3,5 Ah. Par conséquent, il n'est pas nécessaire de parler de différences de cinq ou dix fois dans la capacité des éléments de différents systèmes électrochimiques. Sur la fig. 2 montre une autre série de courbes.
Ils montrent comment la résistance interne des éléments a changé au cours du processus de décharge. La correspondance entre le type d'élément et la couleur de la courbe est la même que sur la Fig. 1. Les valeurs de la résistance interne R, ont été calculées par la formule
où E est la FEM de l'élément ; U - tension sous charge; RH est la résistance de charge. La résistance interne des éléments salins et alcalins augmente de manière monotone à mesure qu'ils sont déchargés. Et la résistance du lithium, ayant fortement diminué au début de la décharge, reste pratiquement inchangée jusqu'à sa toute fin, puis augmente tout aussi fortement. Bien sûr, les expériences réalisées ne peuvent être qualifiées d'exhaustives. La capacité d'un élément n'est pas une valeur strictement fixe, elle dépend de nombreux facteurs externes. Pour différents éléments, son maximum peut être atteint dans des conditions de décharge très différentes. Pour tenir compte de tout cela, une très grande série d'expériences, irréalistes dans des conditions d'amateur, devrait être réalisée. Cependant, essayons de vérifier les résultats obtenus par calcul. Afin d'estimer théoriquement la capacité maximale possible des éléments de divers systèmes électrochimiques, il est nécessaire de connaître la composition chimique de leurs électrodes, de l'électrolyte et de la réaction chimique se produisant dans l'élément. Dans les cellules salines et alcalines, la cathode est le zinc et l'anode est le dioxyde de manganèse. C'est pour cette raison que ces éléments sont appelés collectivement manganèse-zinc. Mais l'électrolyte qu'ils contiennent est différent: sel (généralement chlorure d'ammonium) ou alcali (hydroxyde de potassium). Selon [2], la réaction se produit dans un sel manganèse-zinc élément
et en alcalin
Il n'existe aucune information fiable sur le matériau des électrodes et la réaction chimique dans la pile au lithium. Nous ne pouvons que supposer que les électrodes sont en lithium et en dioxyde de manganèse et que l'électrolyte est une solution de perchlorate de lithium dans du carbonate de propylène. Si cette conjecture est correcte, selon [2], la pile au lithium subit la réaction
En utilisant la loi de Faraday, on obtient une expression pour déterminer la capacité d'une cellule galvanique C, Ah :
où m est la masse des substances en réaction F = 96,5-103 C/g-eq est le nombre de Faraday ; n - valence (pour les cellules galvaniques au sel et alcalines - 2, pour le lithium - 1); M est le poids moléculaire total des réactifs. Nous pesons des cellules galvaniques de taille AA : sel - 17 g, alcalin - 24 g, lithium - 15 g. ) est négligeable et peut être négligée. Nous calculons le poids moléculaire total des substances en réaction à partir des équations de réactions chimiques ci-dessus: pour le sel - 346 g, pour les alcalins - 257 g, pour le lithium - 94 g. En remplaçant les valeurs numériques dans la formule, nous obtenons le maximum possible capacité de l'élément sel - 2,6 Ah , alcalin - 5 Ah, lithium - 4,3 Ah. Les différences entre les valeurs de capacité calculées et celles mesurées peuvent s'expliquer par des hypothèses assez grossières faites dans le calcul. Ainsi, des différences de cinq à dix fois n'ont pas été trouvées. La capacité théorique d'une pile alcaline est environ le double de celle d'une pile au sel, et le lithium n'a aucun avantage sur l'alcaline à cet égard. Ceci est cohérent avec les résultats expérimentaux. Sur la base des résultats de tous les travaux effectués, nous pouvons conclure ce qui suit : 1. Les cellules galvaniques au lithium ont la tension la plus stable, la résistance interne la plus faible, qui ne dépend pratiquement pas du degré de décharge, et la capacité la plus grande, mais pas beaucoup. Il est préférable de les utiliser pour alimenter des équipements à forte consommation de courant, ainsi que dans des appareils qui s'éteignent automatiquement lorsque la tension d'alimentation chute (par exemple, des appareils photo numériques). 2. Les piles alcalines ont une capacité comparable à celle du lithium et sont également capables de fournir un courant élevé à la charge, mais à une tension inférieure. Ils sont mieux utilisés dans les appareils avec une consommation de courant moyenne sans contrôle automatique de la tension. Dans de nombreux cas, les piles alcalines sont préférées au lithium car elles sont trois à quatre fois moins chères. 3. Les cellules de sel ont la capacité la plus petite et la résistance interne la plus élevée. Il est conseillé de les utiliser dans des équipements à faible consommation de courant. littérature
Auteur : I. Podushkin, Moscou
Cuir artificiel pour émulation tactile
15.04.2024 Litière pour chat Petgugu Global
15.04.2024 L’attractivité des hommes attentionnés
14.04.2024
▪ Route en plastique fabriquée à partir de bouteilles recyclées ▪ Drivers LED ISSATA pour luminaires Armstrong ▪ Alimentations de sécurité Mean Well PSC-160 ▪ Dispositif laser produisant des particules de masse négative
▪ section du site Documents de référence. Sélection d'articles ▪ article Pourquoi les Américains s'appellent-ils Pindos ? Réponse détaillée ▪ article IrDA à faire soi-même. Encyclopédie de l'électronique radio et de l'électrotechnique
Commentaires sur l'article : invité Article explicatif, merci.
Page principale | bibliothèque | Articles | Plan du site | Avis sur le site www.diagramme.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






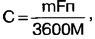
 Laissez votre commentaire sur cet article :
Laissez votre commentaire sur cet article :